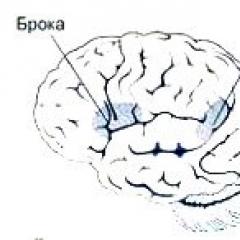
Иммунная система человека: органы, функции и заболевания. Анатомия иммунной и лимфатической систем Клеточный состав иммунной системы организма
Иммунная система является одной из систем жизнеобеспечения, без которой организм не сможет существовать.
Основные функции иммунной системы:
распознавание;
уничтожение;
выведение из организма чужеродных веществ, образующихся в нем и поступающих извне.
Эти функции иммунная система выполняет всю жизнь человека.
Иммунная система человека может характеризоваться наличием врожденных дефектов (так называемые первичные иммунодефициты) или приобретенных в течение жизни под влиянием различных факторов, например, вредного воздействия окружающей среды, стрессовых ситуаций и т. д. Функциональные нарушения иммунной системы могут носить транзиторный характер либо приобретать хроническое течение в виде синдромов иммунологической недостаточности.
Болезни иммунной системы:
Болезни иммунной системы - это нозологические формы с конкретным развитием, четко очерченным патогенезом и клиникой, они объединены понятием иммунодефициты.Изучение болезней иммунной системы началось в середине прошлого столетия после того, как американский врач Брутон выявил у ребенка причину мучающего его гнойного заболевания. Брутон установил, что истоки болезни кроются в имеющемся у ребенка дефекте иммунной системы - агаммаглобулинемии, названного впоследствии синдромом Брутона.
В настоящее время выделены основные разделы иммунологии, изучающие:
функции иммунной системы в норме и патологии;
функции иммунной системы при различных заболеваниях человека;
иммунодефицитные состояния;
болезни иммунной системы;
А также разделы, разрабатывающие:
методы коррекции иммунной системы;
иммунотропные препараты.
Иммунитет подразделяют на 2 вида: естественный (врожденный) и приобретенный, который является специфичным. Естественный иммунитет является неспецифическим по отношению к патогенным агентам. Он представляет собой совокупность защитных факторов, направленных на элиминацию аллергенов. Эти факторы передаются по наследству и являются универсальными, видовыми.
Естественный иммунитет составляют иммунные и неиммунные факторы. К первым относятся барьеры, содержащие различные бактерицидные вещества: кожа, слизистые оболочки, секреты потовых, сальных, слюнных желез, железы желудка, выделяющие соляную кислоту и протеолитические ферменты, а также нормальная микрофлора кишечника. К неиммунным естественным факторам относятся гуморальные факторы (система комплемента, лизоцим, трансферрин и др.) и клеточные факторы (фагоцитарная реакция, работа N К-клеток).
Выделяют 5 групп заболеваний, характеризующихся возникновением патологии иммунной системы:
болезни, связанные с недостаточностью иммунной системы (иммунодефициты первичные, вторичные, транзиторные);
заболевания, связанные с избыточным реагированием иммунной системы;
инфекции иммунной системы;
опухоли иммунной системы.
Иммунная система человека представлена совокупностью органов и тканей, функцией которых является контроль за антигенным постоянством внутренней среды организма. Клетки иммунной системы представлены Т- и В-лимфоцитами, моноцитами, макрофагами, нейтрофилами, эозинофилами, тучными и эпителиальными клетками, фибробластами. Важная роль по обеспечению функции иммунной системы принадлежит иммуноглобулинам, цитокинам, антигенам, рецепторам.
Иммунная система характеризуется многокомпонентностью, но функционирует как единое целое. Она поддерживает клеточное и гуморальное состояния организма.
Для иммунной системы характерны:
мультивариантная регуляция;
открытая система функционирования;
многокомпонентность.
Защита организма посредством иммунной системы происходит за счет специфических и неспецифических элементов защиты с участием биологически активных макромолекул, иммунокомпетентных клеток, органов иммунной системы.
Биологически активными микромолекулами являются:
медиаторы иммунных реакций (интерлейкины);
ростовые факторы (интерфероны опухольнекротизирующих факторов, фактор роста фибробластов, факторы гранулоцитарный, колоннестимулирующий и макрофагальный колоннестимулирующий);
гормоны (пиелопептиды, миелопептиды).
К иммунокомпетентным клеткам относятся:
Т- и В-лимфоциты;
цитотоксические клетки;
предшественники иммунокомпетентных клеток.
Периферическую систему составляют:
селезенка;
лимфатические узлы;
лимфоидные скопления желудочно-кишечного тракта;
кожа;
червеобразный отросток.
Центральные органы иммунитета:
Центральные органы обеспечивают дифференцировку иммунокомпетентных клеток. В области периферических органов происходят иммунологические процессы. Центральные органы иммунитета с возрастом изменяются, а удаление какого-либо органа препятствует возникновению иммунного ответа. Периферические лимфоидные органы сохраняются на протяжении жизни человека и функционируют под воздействием антигенов.Костный мозг:
Костный мозг человека закладывается на 12-13-й недели внутриутробного развития. Костный мозг является источником стволовых клеток, из которых впоследствии развиваются клетки лимфоидной ткани (Т- и В-лимфоциты), а также моноциты и макрофаги. В костном мозге находятся миелоидный и лимфоцитарные ростки. Костный мозг человека содержит 1,5% ретикулярных клеток, 6-7% лимфоцитов, 0,4% плазматических клеток, 60-65% миелоид-ных клеток, 1-3% моноцитов, 26% эритробластов. Стволовые клетки сначала недеференцированны, после 20 недель внутриутробного развития их количество возрастает. »После рождения ребенка костный мозг является единственным местом их образования, производными этих клеток постепенно осуществляется колонизация периферических лимфоидных органов.
В костном мозге образуются многие иммунокомпетентные клетки, кроме этого он является одним из главных источников образования циркулирующих иммуноглобулинов. Динамика образования иммунокомпетентных клеток происходит следующим образом: в желчном мешке эмбриона человека на 2-3-й неделе развития появляется полипотентная стволовая клетка. Между 4-5-й неделями беременности стволовые клетки мигрируют в эмбриональную печень, которая является самым большим кроветворным органом. При этом происходит миграция клеток-предшественников, которые созревают в окружающих их тканях.
Одни клетки-предшественники лимфоидных клеток мигрируют в вилочковую железу, которая возникает на 6-8-й неделе беременности из третьего и четвертого жаберных карманов. Под влиянием эпителиальных клеток кортикального слоя вилочковой железы созревают лимфоциты, которые мигрируют в мозговой слой.
После рождения ребенок сразу встречается с микрофлорой окружающей его среды, перед которой новорожденные и недоношенные дети практически беззащитны. Одним из критических периодов в системе иммунорегуляции является период новорожденности, когда происходит встреча ребенка с антигенами внешнего мира. Вторым критическим периодом является возраст 2-4 месяцев, когда завершается процесс разрушения и выведения антител, прошедших через плаценту, а собственная система В-лимфоцитов остается незрелой.
Часть антител поступает с грудным молоком матери. В этот период происходит увеличение числа клеток, синтезирующих антитела к чужеродным белкам, и главным является наследование особенностей иммунного статуса матери. Вскармливание донорским грудным молоком и искусственное вскармливание делают этот важный процесс невозможным. В период новорожденности сывороточное содержание JgG равно взрослым нормам (10-12 г/л), а уровень JgM и JgA в 40 раз ниже, численность В- и Т-лимфоцитов существенно выше, чем у взрослых, но часть их характеризуется функциональной незрелостью.
Специфическая защита в первые месяцы жизни человека обеспечивается иммуноглобулинами, полученными от матери. Иммуноглобулины М и А поступают с молозивом через пищеварительный тракт ребенка, но в его организме образуются в недостаточном количестве. Нарастание антител происходит в возрасте 14-16 лет.
Способность защиты путем иммунных реакций формируется во внутриутробном периоде развития и становится выраженной к концу первого года жизни. Т-лимфоциты превращаются в сенсибилизированные активные лимфоциты, а В-лимфоциты в плазматические клетки, создающие специфические иммуноглобулины.
Способность организма отвечать иммунной реакцией на чужеродные антигены активно приобретается после перенесенных инфекций или вакцинаций и целиком зависит от работы иммунокомпетентных клеток (Т- и В-лимфоцитов), которые образуются в вилочковой железе и костном мозге и с помощью рецепторов распознают чужеродные антигены.
Красный костный мозг:
Красный костный мозг располагается внутри костей. Он может находиться как в активном, так и неактивном состоянии. У детей младшего возраста все кости содержат активный костный мозг, у детей старших возрастов и взрослых активный костный мозг располагается в плоских костях (черепе, ребрах, грудине, малом тазу).У взрослых красный костный мозг при определенных условиях может переходить в активное состояние с образованием дополнительного числа клеток крови. В красном костном мозге происходит постоянное воспроизводство клеток: красных кровяных телец (эритроцитов) и лейкоцитов, поскольку отмирающие клетки заменяются новыми. Каждый тип клеток имеет разную скорость образования.
Красный костный мозг рассматривается как отдельный орган, который участвует в образовании красных и белых кровяных телец и обеспечивает нормальное функционирование иммунной системы.
Вилочковая железа (зобная железа, тимус):
Другим важным органом иммунной системы является вилочковая железа (зобная железа, тимус), обеспечивающая становление и функционирование системы иммунитета. Она образуется на первом месяце внутриутробного развития. К рождению ребенка вилочковая железа состоит из двух долей, которые соединены перешейком. В долях располагаются корковое и мозговое вещества. Корковое вещество состоит из тимоцитов, в мозговом веществе располагаются эпителиальные элементы, среди которых имеются тельца Гассаля.Масса вилочковой железы с возрастом увеличивается (к 3 годам), в возрасте 12-15 лет она достигает массы 30 г, после чего происходит ее инволюция с замещением железистой ткани железы жировой и соединительной.
Вилочковая железа - железа внутренней секреции. Она участвует в лимфопоэзе и иммунологических защитных реакциях организма, являясь центральным органом клеточного иммунитета.
В вилочковой железе происходит образование биологически активных веществ и гормонов, таких как:
тимозин - гормон, индуцирующий экспрессию Т-клеточных рецепторов, восстанавливает иммунологическую компетентность;
фактор со свойствами холинэстеразы, который блокирует передачу импульсов на мышечное волокно с возникновением миотопического синдрома. Снижение выработки данного фактора может привести к холинергическому кризу;
тимоноэтин-2 - увеличивает содержание АМФ в лимфоцитах, усиливает экспрессию Т-клеточных антигенов на цитомембранах клеток костного мозга;
убивикин принимает участие в экспрессии на Т-и В-лимфоцитах, синтез антител и других лимфоцитостимулирующих факторах;
тимический гормон, который является антагонистом АКТГ;
тимический гипокальциемический фактор.
Патология вилочковой железы приводит к возникновению ряда синдромов и заболеваний: аплазии, гипоплазии, гиперплазии, различных опухолей. Встречаются также люди с врожденным отсутствием тимуса.
Эти состояния сопровождаются признаками Т-клеточной иммунологической недостаточности, гипокальциемическими судорогами и другими симптомами.
Селезенка:
Селезенка является фильтрующим аппаратом, обеспечивающим детоксикацию, удаление старых эритроцитов и других клеток, в ней происходит дифференцировка старых и поврежденных эритроцитов, лимфоцитов; образуются антитела.В селезенке образуется тафтсин, основная функция которого заключается в повышении миграции, фагоцитарной активности макрофагов и нейтрофилов. Он увеличивает цитотоксическое действие Т-лимфоцитов, стимулирует синтез антител. По строению тафтсин напоминает фрагмент иммуноглобулинов, в связи с этим введение иммуноглобулинов компенсирует дефицит тафтсина.
Лимфатическая система:
Лимфатическая система обладает неспецифической барьерной функцией. Она является местом развития иммунного ответа - как клеточного, так и гуморального. У человека насчитывается около тысячи лимфатических узлов, которые обеспечивают регионарную защиту организма от попадания в него инфекционных и неинфекционных начал. В нормальных условиях лимфоузлы не пальпируются. При различных заболеваниях, опухолях, а также при наличии хронических очагов инфекции, они увеличиваются в размерах и легко пальпируются. При клеточном варианте иммунной недостаточности может возникнуть гипоплазия лимфатической системы, включая гемоплазию тимуса, небных миндалин, лимфатических узлов.Все группы лимфатических узлов увеличиваются в случае поликлональной активации В-лимфоцитов с увеличением продукции иммуноглобулинов, в том числе иммуноглобулинов М. Для хронических инфекций с недостаточной функцией Т-лимфоцитов-хелперов, от которых зависит переключение синтеза антител с JgM класса на JgG, характерен переход в злокачественные варианты лимфопролиферативных состояний.
У детей в возрасте от 1 года до 10-12 лет часто встречается реакция в виде микрополиаденита.
Небные миндалины располагаются в полости рта и обеспечивают защиту верхних дыхательных путей от инфекции, снабжают иммунокомпетентными клетками лимфатическую систему, принимают участие в формировании микробной флоры полости /га. Небные миндалины функционируют в тесной связи с/вилочковой железой, тимэктомия приводит к гипертрофии миндалин, тонзилэктомия - к атрофии тимуса. Гиперплазия миндалин может привести к клеточным вариантам иммунной недостаточности. С возрастной инволюцией тимуса происходит инволюция и атрофия миндалин. Часто увеличение вилочковой железы сочетается с гипертрофией миндалин и клеточной иммунологической недостаточностью.
Пейеровы бляшки располагаются в кишечнике, они принимают участие в созревании Т- и В-лимфоцитов и формировании иммунного ответа. В случае атрофии пейеровых бляшек происходит нарушение в процессе созревания Т-лимфоцитов. Хотя кровь не относится к лимфатической системе, лабораторные исследования крови дают сведения о наличии лимфоцитов, образующихся в лимфоидной ткани, состоящей из ретикулярных и лимфоидных клеток.
>> анатомия и физиология
Иммунитет (от лат. immunitas – освобождать от чего-либо) – это физиологическая функция, которая обуславливает невосприимчивость организма к чужеродным антигенам. Иммунитет человека делает его невосприимчивым по отношению ко многим бактериям, вирусам, грибкам, глистам, простейшим, различным ядам животных. Кроме того, иммунитет обеспечивает защиту организма от раковых клеток.
Задачей иммунной системы является распознавать и разрушать все чужеродные структуры. При контакте с чужеродной структурой клетки иммунной системы запускают иммунный ответ , который приводит к выведению чужеродного антигена из организма.
Функция иммунитета обеспечивается работой иммунной системы организма, в состав которой входят различные типы органов и клеток. Ниже рассмотрим подробнее строение иммунной системы и основные принципы ее функционирования.
Анатомия иммунной системы
Анатомия иммунной системы чрезвычайно неоднородна. В целом, клетки и гуморальные факторы иммунной системы присутствуют почти во всех органах и тканях организма. Исключение составляют некоторые отделы глаз, яичек у мужчин, щитовидной железы , головного мозга – эти органы ограждены от иммунной системы тканевым барьером, который необходим для их нормального функционирования.
В общем, работа иммунной системы обеспечивается двумя видами факторов: клеточными и гуморальными (то есть жидкостными). Клетки иммунной системы (различные виды лейкоцитов) циркулируют в крови и переходят в ткани, осуществляя постоянный надзор за антигенным составов тканей. Кроме того, в крови циркулирует большое количество разнообразных антител (гуморальные, жидкостные факторы), которые также способны распознавать и уничтожать чужеродные структуры.
В архитектуре иммунной системы различаем центральные и периферические структуры. Центральными органами иммунной системы являются костный мозг и тимус (вилочковая железа). В костном мозге (красный костный мозг) происходит формирование клеток иммунной системы из так называемых стволовых клеток , которые дают начало всем клеткам крови (эритроциты, лейкоциты, тромбоциты). Вилочковая железа (тимус) расположена в грудной клетке, сразу позади грудины. Тимус хорошо развит у детей, но с возрастом подвергается инволюции и практически отсутствует у взрослых. В тимусе происходит дифференциация лимфоцитов – специфических клеток иммунной системы. В процессе дифференциации лимфоциты «учатся» распознавать «свои» и «чужие» структуры.
Периферические органы иммунной системы представлены лимфатическими узлами, селезенкой и лимфоидной тканью (такая ткань находится, например, в небных миндалинах, на корне языка, на задней стенке носоглотки, в кишечнике).
Лимфатические узлы представляют собой скопление лимфоидной ткани (на самом деле скопление клеток иммунной системы) окруженные оболочкой. В лимфатический узел входят лимфатические сосуды, по которым течет лимфа. Внутри лимфатического узла лимфа фильтруется и очищается от всех чужеродных структур (вирусы , бактерии , раковые клетки). Сосуды выходящие из лимфатического узла сливаются в общий проток, который впадает в вену.
Селезенка представляет собой не что иное, как большой лимфатический узел. У взрослого человека масса селезенки может достигать нескольких сотен граммов, в зависимости от количества крови, накопленного в органе. Селезенка расположена в брюшной полости слева от желудка. В сутки через селезенку прокачивается большое количество крови, которая, подобно лимфе в лимфатических узлах, подвергается фильтрации и очищению. Также в селезенке запасается определенное количество крови, в котором организм на данный момент не нуждается. Во время физической нагрузки или стресса селезенка сокращается и выбрасывает кровь в кровеносные сосуды, для того чтобы удовлетворить потребность организма в кислороде.
Лимфоидная ткань рассеяна по всему организму в виде маленьких узелков. Основная функция лимфоидной ткани – обеспечение местного иммунитета, поэтому наиболее крупные скопления лимфоидной ткани расположены в области рта, глотки и кишечника (эти зоны организма в изобилии населены разнообразными бактериями).
Кроме того, в различных органах существуют, так называемые, мезенхимальные клетки , которые могут выполнять иммунную функцию. Много таких клеток в коже, печени, почках .
Клетки иммунной системы
Общее название клеток иммунной системы это лейкоциты
. Однако семейство лейкоцитов очень неоднородно. Различаем два основных типа лейкоцитов: зернистые и незернистые.
Нейтрофилы – наиболее многочисленные представители лейкоцитов. Эти клетки содержат вытянутое ядро, разделенное на несколько сегментов, поэтому иногда их называют сегментоядерными лейкоцитами. Как и все клетки иммунной системы, нейтрофилы образуются в красном костном мозге и после созревания попадают в кровь. Время циркуляции нейтрофилов в крови не велико. В течение нескольких часов эти клетки проникают через стенки сосудов и переходят в ткани. Пробыв некоторое время в тканях, нейтрофилы могут вновь вернуться в кровь. Нейтрофилы чрезвычайно чувствительны к наличию в организме очага воспаления и способны направленно мигрировать в воспаленные ткани. Попадая в ткани, нейтрофилы меняют свою форму – из круглых превращаются в отростчатые. Основная функция нейтрофилов обезвреживание различных бактерий. Для передвижения в тканях нейтрофил снабжен своеобразными ножками, которые представляют собой выросты цитоплазмы клетки. Придвигаясь к бактерии нейтрофил, окружает ее своими отростками, а затем «заглатывает» и переваривает ее при помощи специальных ферментов. Отмершие нейтрофилы скапливаются в очагах воспаления (например, в ранах) в виде гноя. Количество нейтрофилов крови увеличивается во время различных воспалительных заболеваний бактериальной природы.
Базофилы принимают активное участие в развитии аллергических реакций немедленного типа. Попадая в ткани базофилы, превращаются в тучные клетки, содержащие большое количество гистамина – биологически активного вещества, которое стимулирует развитие аллергии. Благодаря базофилам яды насекомых или животных сразу блокируются в тканях и не распространяются по всему телу. Также базофилы регулируют сворачиваемость крови при помощи гепарина.
Лимфоциты . Существует несколько разновидностей лимфоцитов: B-лимфоциты (читается «Б-лимфоциты»), Т-лимфоциты (читается «Т-лимфоциты»), К-лимфоциты (читается «К-лимфоциты»), NK-лимфоциты (естественные киллеры) и моноциты.
В-лимфоциты распознают чужеродные структуры (антигены) вырабатывая при этом специфические антитела (белковые молекулы, направленные против чужеродных структур).
Т-лимфоциты выполняют функцию регуляции иммунитета. Т-помошники стимулируют выработку антител, а Т-супрессоры тормозят ее.
К-лимфоциты способны разрушать чужеродные структуры, помеченные антителами. Под влиянием этих клеток могут быть разрушены различные бактерии, раковые клетки или клетки инфицированные вирусами.
NK-лимфоциты осуществляют контроль над качеством клеток организма. При этом NK-лимфоциты способны разрушать клетки, которые по своим свойствам отличаются от нормальных клеток, например, раковые клетки.
Моноциты это самые большие клетки крови. Попадая в ткани, они превращаются в макрофагов. Макрофаги это большие клетки, активно разрушающие бактерии. Макрофаги в больших количествах накапливаются в очагах воспаления.
По сравнению с нейтрофилами (см. выше) некоторые виды лимфоцитов более активны в отношении вирусов, чем бактерий, и не разрушаются во время реакции с чужеродным антигеном, поэтому в очагах воспаления вызванного вирусами гной не формируется. Также лимфоциты накапливаются в очагах хронического воспаления.
Популяция лейкоцитов постоянно обновляется. Каждую секунду образуются миллионы новых иммунных клеток. Некоторые клетки иммунной системы живут всего несколько часов, а другие могут сохраняться на протяжении нескольких лет. В этом и заключается суть иммунитета: однажды повстречав антиген (вирус или бактерию), иммунная клетка «запоминает» его и при новой встрече реагирует быстрее, блокируя инфекцию сразу после ее попадания в организм.
Общая масса органов и клеток иммунной системы организма взрослого человека составляет около 1 килограмма . Взаимодействия между клетками иммунной системы чрезвычайно сложны. В целом, согласованная работа различных клеток иммунной системы, обеспечивает надежную защиту организма от различных инфекционных агентов и собственных мутировавших клеток.
Помимо функции защиты иммунные клетки контролируют рост и размножение клеток организма, а также восстановление тканей в очагах воспаления.
Кроме клеток иммунной системы в организме человека существует ряд факторов неспецифической защиты, которые составляют так называемый видовой иммунитет. Эти факторы защиты представлены системой комплимента, лизоцимом, трансферином, С-реактивным белком, интерферонами.
Лизоцим – это специфический фермент, который разрушает стенки бактерий. В больших количествах лизоцим содержится в слюне, чем объясняются ее антибактериальные свойства.
Трансферин – это белок, который конкурирует с бактериями за захват определенных веществ (например, железо), необходимых для их развития. В результате этого рост и размножение бактерий замедляется.
С-реактивный белок активируется подобно комплименту при попадании в кровь чужеродных структур. Присоединение этого белка к бактериям делает их уязвимыми для клеток иммунной системы.
Интерфероны – это сложномолекулярные вещества, которые выделяются клетками в ответ на проникновение в организм вирусов. Благодаря интерферонам клетки становятся невосприимчивыми по отношению к вирусу.
Библиография :
- Хаитов Р.М. Иммуногенетика и иммунология, Ибн Сина, 1991
- Лесков,В.П. Клиническая иммунология для врачей, М., 1997
- Борисов Л.Б. Медицинская Микробиология, вирусология, иммунология, М. : Медицина, 1994
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Центральными органами иммунной системы являются костный мозг и тимус.
Костный мозг – орган кроветворения и центральный орган иммунной системы. Выделяют красный костный мозг, который у взрослого человека располагается в ячейках губчатого вещества плоских и коротких костей, а также в эпифизах трубчатых костей, и желтый костный мозг, заполняющий полости в диафизах трубчатых костей. В детском возрасте все костномозговые полости заполнены красным костным мозгом. Общая масса костного мозга составляет 2,5 – 3 кг (от 4 до 5% массы тела). Красный костный мозг состоит из миелоидной (кровеобразующей) и лимфоидной ткани. В красном костном мозге находятся также стволовые клетки – родоначальники всех видов клеток крови и иммунной системы, обладающие способностью к многократному (до 100 раз) делению.
Тимус располагается позади тела грудины. Он состоит из двух удлиненных асимметричных по величине правой и левой долей. Каждая доля разделена на многочисленные дольки размером от 1 до 10 мм. Периферию долек образует более темное корковое вещество, а центральную часть – более светлое мозговое вещество. Строма тимуса образована многоотросчатыми эпителиоретикулоцитами, формирующими сеть, в петлях которой располагаются Т-лимфоциты и их предшественники. Эпителиоретикулоциты вырабатывают биологически активные вещества (тимозин, тимопоэтин), которые оказывают влияние на дифференцировку Т-лимфоцитов. В мозговом веществе Эпителиоретикулоциты образуют слоистые структуры – химические тельца (тельца Гассаля). Образование Т-лимфоцитов происходит преимущественно в корковом веществе, откуда они перемещаются в мозговое вещество и мигрируют в кровеносное русло.
К периферическим органам иммунной системы относят нёбные, трубные, глоточную и язычную миндалины, которые образуют глоточное лимфоидное кольцо Пирогова - Вальдейера. Миндалины представляют собой скопление лимфоидной ткани, в которой располагаются небольших размеров структуры (0,2 – 1 мм) с плотно расположенными в них лимфоцитами – лимфоидные узелки.
Нёбная миндалина (парная) – самая крупная. Она расположена с обеих сторон зева. На свободной поверхности миндалин, обращенной в сторону зева и покрытой многослойным плоским эпителием, видны мелкие, точечной величины миндалиновые отверстия миндалиновых крипт. Стенки многочисленных миндалиновых крипт существенно увеличивают площадь поверхности миндалин, соприкасающейся с проходящей в глотку пищей и вдыхаемым воздухом.
Трубная миндалина (парная) представляет собой скопление лимфоидной ткани в слизистой оболочке вокруг глоточного отверстия слуховой трубы. Глоточная миндалина (непарная) располагается в слизистой оболочке верхней стенки глотки против хоан, сообщающих полость носа с носоглоткой. Язычная миндалина (непарная) находится в слизистой оболочке корня языка.
Вес шесть миндалин окружают вход в глотку из полости рта и из носовой полости. Именно здесь, на поверхности миндалин, происходит первая встреча лимфоцитов с чужеродными веществами и микроорганизмами, оказавшимися в проглатываемой пище или во вдыхаемом воздухе.
Одиночные лимфоидные узелки, располагающиеся в слизистой оболочке органов пищеварительной, дыхательной систем и мочевыводящих путей, представляют собой плотные скопления лимфоцитов, образующие структуры шаровидной или яйцевидной формы. Залегая под эпителием слизистой оболочки на близком расстоянии друг от друга, лимфоидные узелки, как сторожевые посты, защищают слизистую оболочку и организм в целом от проникновения в нее генетически чужеродных частиц и микроорганизмов. Внутри многих лимфоидных узелков образуются собственные центры размножения. В случае антигенной опасности начинается быстрое размножение лимфоцитов в лимфоидных узелках.
В слизистой оболочке тонкой кишки расположены лимфоидные бляшки, представляющие собой скопления лимфоидных узелков. Лимфоидные бляшки, как правило, имеют овальную форму и чуть-чуть выступают в просвет кишки. На месте лимфоидных бляшек ворсинки слизистой оболочки отсутствуют. Лимфоидные бляшки в тонкой кишке, где происходит основное всасывание продуктов переваривания пищи, препятствуют проникновению в кровеносное и лимфатическое русло чужеродных веществ.
Рис. 92. Строение лимфатического узла:
1 – капсула, 2 – капсулярная трабекула, 3 – приносящий лимфатический сосуд, 4 – подкапсулярный (краевой) синус, 5 – корковое вещество, 6 – паракортикальная (тимусзависимая) зона (околокорковое вещество), 7 – лимфоидный узелок, 8 – центр размножения, 9 – вокругузелковый корковый синус, 10 – мозговое вещество (мякотные тяжи), 11 – мозговые синусы, 12 – воротный синус, 13 – выносящий лимфатический сосуд, 14 – ворота, 15 – кровеносные сосуды
Червеобразный отросток – аппендикс также является органом иммунной системы. В его стенках имеется огромное количество лимфоидных узелков (до 550), плотно прилежащих друг к другу. Аппендикс расположен на границе между тонкой и толстой кишкой, является важным органом в функциях иммунной защиты организма.
Лимфатические узлы расположены на путях тока лимфы от органов и тканей к лимфатическим стволам и протокам. В лимфатических узлах задерживаются и уничтожаются чужеродные частицы, микробные тела, собственные погибшие клетки, попавшие в просвет лимфатических сосудов в момент всасывания в них тканевой жидкости. Лимфатические узлы располагаются группами, состоящими из двух и более узлов.
Каждый лимфатический узел имеет соединительнотканную капсулу, от которой внутрь узла отходят пучки соединительной ткани – трабекулы (рис. 92).
В паренхиме лимфатического узла выделяют корковое и мозговое вещество. Корковое вещество занимает периферические отделы узла. В корковом веществе расположены лимфоидные узелки.
В центральных отделах лимфатического узла находится мозговое вещество. Паренхима мозгового вещества представлена тяжами лимфоидной ткани – мякотными тяжами, которые простираются от внутренних отделов коркового вещества до ворот лимфатического узла. Пограничная с мозговым веществом часть коркового вещества получила название паракортикальной или тимусзависимой зоны.
Под капсулой лимфатического узла, а также вдоль соединительнотканных трабекул и мякотных тяжей лежат узкие щели – лимфатические синусы, внутри которых находятся мелкоячеистые сети, образованные ретикулярными волокнами. По этим синусам течет лимфа от приносящих сосудов к выносящим лимфатическим сосудам. Во время тока лимфы по синусам сквозь сети из ретикулярных волокон задерживаются погибшие клетки, микробные тела и другие чужеродные вещества, присутствующие в лимфе. Все эти чужеродные вещества распознаются и уничтожаются лимфоцитами, проникающими внутрь синусов из лимфоидной паренхимы.
Таким образом, лимфатические узлы задерживают любые чужеродные частицы, которые попали в организм, и препятствуют их проникновению из органов и тканей в ток крови.
Селезенка располагается в брюшной полости в левом подреберье. Это единственный орган, контролирующий состав крови. Масса селезенки составляет 150 – 200 г. Снаружи она имеет соединительнотканную капсулу, от которой внутрь органа отходят трабекулы. Между трабекулами находится мякоть селезенки, ее пульпа. Выделяют белую и красную пульпы, в которых разветвляются артериальные сосуды – пульпарные артерии. Белая пульпа представлена типичной лимфоидной тканью, включает расположенные вокруг пульпарных артерий периартериальные лимфоидные муфты, лимфоидные узелки и эллипсоиды, окружающие кровеносные капилляры. Красная пульпа, занимающая до 78% всего объема селезенки, состоит из ретикулярной стромы, в петлях которой находятся лимфоциты, лейкоциты, макрофаги, погибшие эритроциты и другие клетки.
Образованные этими клетками тяжи располагаются между селезеночными венозными синусами. Протекающая по пульпарным артериям кровь контролируется лимфоидными клетками периартериальных лимфоидных муфт, эллипсоидов и лимфоидных узелков. Распознанные чужеродные элементы в синусах селезенки захватываются макрофагами, которые переносят их в красную пульпу. Здесь они уничтожаются. Продукты уничтожения чужеродных веществ поступают по воротной вене с кровью в печень, где они утилизируются.
Похожая информация.
Основная функция иммунной системы - контроль за качественным постоянством генетически продетерминированного клеточного и гуморального состава организма.
Иммунная система обеспечивает:
Защиту организма от внедрения чужеродных клеток и от возникших в организме модифицированных клеток (например, злокачественных);
Уничтожение старых, дефектных и поврежденных собственных клеток, а также клеточных элементов, не характерных для данной фазы развития организма;
Нейтрализацию с последующей элиминацией всех генетически чужеродных для данного организма высокомолекулярных веществ биологического происхождения (белков, полисахаридов, липополисахаридов и т.д.).
В иммунной системе выделяют центральные (тимус и костный мозг) и периферические (селезенка, лимфатические узлы, скопления лимфоидной ткани) органы, в которых осуществляется дифференцировка лимфоцитов в зрелые формы и происходит иммунный ответ.
Функционирующей основой иммунной системы является сложный комплекс иммунокомпетентных клеток (Т-, В-лимфоциты, макрофаги).
Т-лимфоциты происходят из полипотентных костномозговых клеток. Дифференциация стволовых клеток в Т-лимфоциты индуцируется в тимусе под влиянием тимозина, тимостимулина, тимопоэтинов и других гормонов, которые продуцируются звездчатыми эпителиальными клетками или тельцами Гассаля. По мере созревания у пре-Т-лимфоцитов (претимических лимфоцитов) происходит приобретение антигенных маркеров. Заканчивается дифференциация появлением у зрелых Т-лимфоцитов специфического рецепторного аппарата распознавания антигенов. Образовавшиеся Т-лимфоциты через лимфу и кровь колонизируют тимусзависимые паракортикальные зоны лимфатических узлов или соответствующие зоны лимфоидных фолликулов селезенки.
По функциональным свойствам популяция Т-лимфоцитов разнородна. В соответствии с международной классификацией основные антигенные маркеры лимфоцитов обозначены как кластеры дифференцировки или CD (от англ. cluster differentiation). Соответствующие наборы моноклональных антител позволяют выявлять лимфоциты, несущие конкретные антигены. Зрелые Т-лимфоциты обозначаются маркером CD3+, являющимся частью Т-клеточного рецепторного комплекса. По функциям среди Т-лимфоцитов различают супрессорные/цитотоксические клетки CD8+, Т-лимфоциты индукторы/хелперы CD4+, CD16+ - естественные киллеры.
Особенность Т-клеточного рецептора – способность распознавать чужеродный антиген только в комплексе с собственными клеточными антигенами на поверхности вспомогательных антиген-представляющих клеток (дендритных или макрофагов). В отличие от В-лимфоцитов, способных распознавать антигены в растворе и связывать белковые, полисахаридные и липопротеидные растворимые антигены, Т-лимфоциты способны распознать только короткие пептидные фрагменты белковых антигенов, представленные на мембране других клеток в комплексе с собственными антигенами главного комплекса гистосовместимости MHC (от английского Major Histocompatibility Complex).
CD4+ Т-лимфоциты способны распознавать антигенные детерминанты в комплексе с MHC молекулами II класса. Они выполняют посредническую сигнальную функцию, передавая информацию об антигенах иммунокомпетентным клеткам. В гуморальном иммунном ответе Т-хелперы реагируют с несущей частью тимусзависимого антигена, индуцируя превращение В-лимфоцитов в плазмоциты. В присутствии Т-хелперов синтез антител усиливается на один-два порядка. Т-хелперы индуцируют образование цитотоксических/супрессорных Т-лимфоцитов. Т-хелперы - долгоживущие лимфоциты, чувствительны к циклофосфамиду, содержат рецепторы к митогенам. После распознавания антигена CD4+ лимфоциты могут дифференцироваться в различных направлениях с формированием Т-хелперов 1-го, 2-го и 3-го типов.
CD8+ Т-лимфоциты являются регуляторами антителообразования и других иммунных процессов, участвуют в формировании иммунологической толерантности; их цитотоксическая функция состоит в способности разрушать инфицированные и злокачественно перерожденные клетки. Эти клетки способны распознавать широкий спектр антигенных детерминант, что можно объяснить низким порогом активации их рецепторного аппарата или наличием нескольких специфических рецепторов. Как и все другие субпопуляции тимоцитов, CD8+ содержат рецепторы к митогенам. Очень чувствительны к ионизирующей радиации и имеют короткий период жизни.
Естественные киллеры распознают антигенные детерминанты в комплексе с МНС молекулами II класса, являются долгоживущими клетками, устойчивы к циклофосфамиду, очень чувствительны к радиации, имеют рецепторы к Fc-фрагменту антител.
Клеточная стенка В-лимфоцитов в своем составе имеет рецепторы CD19, 20, 21, 22. В-клетки происходят от стволовых клеток. Созревают они поэтапно - первоначально в костном мозге, затем в селезенке. На самой ранней стадии созревания на цитоплазматической мембране В-клеток экспрессируются иммуноглобулины класса М, несколько позже - в комплексе с ними появляются иммуноглобулины G или А, а к моменту рождения, когда происходит полное созревание В-лимфоцитов - иммуноглобулины D. Возможно, у зрелых В-лимфоцитов на цитоплазматической мембране присутствуют сразу три иммуноглобулина - М, G, D или М, А, D. Эти рецепторные иммуноглобулины не секретируются, но могут слущиваться с мембраны.
Так как большинство антигенов тимусзависимые, то для трансформации незрелых В-лимфоцитов в антителопродуцирующие обычно недостаточно одного антигенного стимула. При попадании таких антигенов в организм В-лимфоциты дифференцируются в плазмоциты с помощью Т-хелперов при участии макрофагов и стромальных ретикулярных отростчатых клеток. При этом хелперы выделяют цитокины (ИЛ-2) - гуморальные эффекторы, которые и активируют пролиферацию В-лимфоцитов. Независимо от природы и силы антигена, который вызвал трансформацию В-лимфоцитов, образующиеся плазмоциты продуцируют антитела, специфичность которых аналогична рецепторным иммуноглобулинам. Таким образом, антигенный стимул надо рассматривать как пусковой сигнал для выработки генетически запрограммированного синтеза антител.
Макрофаги - основной тип клеток моноцитарной системы лимфоцитов. Они представляют собой гетерогенные по функциональной активности долгоживущие клетки с хорошо развитой цитоплазмой и лизосомальным аппаратом. На их поверхности имеются специфические рецепторы к В- и Т-лимфоцитам, Fc-фрагменту иммуноглобулина G, С3b-компоненту комплемента, цитокинам, гистамину. Различают подвижные и фиксированные макрофаги. Те и другие дифференцируются из стволовой кроветворной клетки через стадии монобласта, промоноцита, превращаясь в подвижные моноциты крови и фиксированные (альвеолярные макрофаги дыхательных путей, купферовские клетки печени, париетальные макрофаги брюшины, макрофаги селезенки, лимфатических узлов).
Значение макрофагов как антигенпрезентирующих клеток состоит в том, что они накапливают и подвергают переработке проникающие в организм тимусзависимые антигены и презентируют (представляют) их в трансформированном виде для распознавания тимоцитами, вслед за чем стимулируется пролиферация и дифференциация В-лимфоцитов в антителопродуцирующие плазмоциты. При определенных условиях макрофаги проявляют цитотоксическое действие на опухолевые клетки. Они также секретируют интерферон, ИЛ-1, ФНО-альфа, лизоцим, различные компоненты комплемента, факторы, дифференцирующие стволовые клетки в гранулоциты, стимулирующие размножение и созревание Т-лимфоцитов.
Антитела - это особый вид белков, называемых иммуноглобулинами (Ig), которые вырабатываются под влиянием антигенов и обладают способностью специфически связываться с ними. При этом антитела могут нейтрализовать токсины бактерий и вирусы (антитоксины и вируснейтрализующие антитела), осаждать растворимые антигены (преципитины), склеивать корпускулярные антигены (агглютинины), повышать фагоцитарную активность лейкоцитов (опсонины), связывать антигены, не вызывая каких-либо видимых реакций (блокирующие антитела), совместно с комплементом лизировать бактерии и другие клетки, например, эритроциты (лизины).
На основании различий в молекулярной массе, химических свойствах и биологической функции выделяют пять основных классов иммуноглобулинов: IgG, IgM, IgA, IgE и IgD.
Цельная молекула иммуноглобулина (или его мономера у IgA и IgM) состоит из трех фрагментов: двух Fab-фрагментов, каждый из которых включает вариабельный участок тяжелой цепи и связанную с ним легкую цепь (на концах Fab-фрагментов находятся гипервариабельные участки, формирующие активные центры связывания антигенов), и одного Fc-фрагмента, состоящего из двух константных участков тяжелых цепей.
Иммуноглобулины класса G составляют около 75% всех иммуноглобулинов сыворотки крови человека. Молекулярная масса IgG минимальна - 150 000 Да, что обеспечивает ему возможность проникновения через плаценту от матери к плоду, с чем и связано развитие трансплацентарного иммунитета, защищающего организм ребенка от многих инфекций в первые 6 месяцев жизни. Молекулы IgG - наиболее долгоживущие из всех (период полураспада в организме составляет 23 дня). Антитела этого класса особенно активны против грамотрицательных бактерий, токсинов и вирусов.
IgM - эволюционно самый старый класс иммуноглобулинов. Содержание его в сыворотке крови составляет 5-10% от общего количества иммуноглобулинов. IgM синтезируется при первичном иммунном ответе: в начале ответа появляются антитела класса М, и лишь через 5 сут начинается синтез антител класса IgG. Молекулярная масса сывороточного IgM 900 000 Да.
IgA, составляющий 10-15% от всех иммуноглобулинов сыворотки крови, является обычно преобладающим иммуноглобулином секретов (слизистых выделений дыхательных путей, желудочно-кишечного тракта, слюны, слез, молозива и молока). Секреторный компонент IgA образуется в эпителиальных клетках и выходит на их поверхность, где присутствует в качестве рецептора. IgA, выходя из кровотока через капиллярные петли и проникая через эпителиальный слой, соединяется с секреторным компонентом. Образовавшийся секреторный IgA остается на поверхности эпителиальной клетки или сползает в слой слизи над эпителием. Здесь он осуществляет свою основную эффекторную функцию, состоящую в агрегации микробов и сорбции этих агрегатов на поверхности эпителиальных клеток с одновременным угнетением размножения микробов, чему способствует лизоцим и, в меньшей степени, комплемент. Молекулярная масса IgA около 400 000 Да.
IgE является минорным классом иммуноглобулинов: его содержание составляет всего около 0,2% от всех сывороточных иммуноглобулинов. Молекулярная масса IgE около 200 000 Да. IgE накапливается преимущественно в тканях слизистых и кожных оболочек, где сорбируется за счет Fc-рецепторов на поверхности тучных клеток, базофилов и эозинофилов. В результате присоединения специфического антигена происходит дегрануляция этих клеток и выброс биологически активных веществ.
IgD также представляет минорный класс иммуноглобулинов. Его молекулярная масса 180 000 Да. Отличается он от IgG только в тонких деталях структуры молекулы.
Ведущую роль в регуляции антигенпредставления, активности иммуноцитов и воспаления играют цитокины – универсальные медиаторы межклеточного взаимодействия. Они могут непосредственно вырабатываться в ЦНС и имеют рецепторы на клетках нервной системы.
Цитокины делятся на две большие группы – провоспалительные и противовоспалительные. К провоспалительным относятся ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-12, ФНО-альфа, к противовоспалительным – ИЛ-4, ИЛ-10, ИЛ-13 и ТРФ-бета.
Основные эффекты цитокинов и их продуценты.
(И.С.Фрейндлин, 1998, с изменениями)
К цитокинам относятся и интерфероны, обладающие множеством биологических активностей, проявляющихся в противовирусном, противоопухолевом и иммуностимулирующем действии. Они блокируют внутриклеточную репликацию вируса, подавляют клеточное деление, стимулируют активность естественных киллеров, повышают фагоцитарную активность макрофагов, активность поверхностных антигенов гистосовместимости и в то же время тормозят созревание моноцитов в макрофаги.
Интерферон-альфа (ИФН-альфа) продуцируется макрофагами и лейкоцитами в ответ на вирусы, клетки, инфицированные вирусом, злокачественные клетки и митогены.
Интерферон-бета (ИФН-бета) синтезируется фибробластами и эпителиальными клетками под действием вирусных антигенов и самого вируса.
Интерферон-гамма (ИФН-гамма) продуцируется активированными Т-лимфоцитами в результате действия индукторов (Т-клеточные митогены, антигены). Для продукции ИФН-гамма требуются акцессорные клетки – макрофаги, моноциты, дендритные клетки.
Основные эффекты интерферонов.

Каждый тип клеток характеризуется наличием на их мембране основных форм адгезивных молекул. Так, иммунные клетки идентифицируются по их рецепторам (например, CD4, CD8 и т.д.). Под воздействием различных стимулов (цитокиновая стимуляция, токсины, гипоксия, термические и механические воздействия и т.п.) клетки способны увеличивать плотность некоторых рецепторов (например, ICAM-1, VFC-1, CD44), а также экспрессировать новые типы рецепторов. В зависимости от функциональной активности клетки периодически изменяют вид и плотность поверхностных молекул. Эти феномены наиболее выражены у иммунокомпетентных клеток.
Наиболее активно изучена роль межклеточной молекулы адгезии-1 (ICAM-1), которая экспрессируется на эндотелии сосудов мозга. Эта молекула играет основную роль в адгезии активированных лимфоцитов крови к эндотелию и в их последующем проникновении в ткань мозга. Воспалительные цитокины способны стимулировать экспрессию гена ICAM-1 и синтез этой молекулы в астроцитах.
Выделяют две основные формы специфического иммунного ответа – клеточный и гуморальный.
Клеточный иммунный ответ подразумевает накопление в организме клона Т-лимфоцитов, несущих специфические для данного антигена антиген-распознающие рецепторы и ответственных за клеточные реакции иммунного воспаления – гиперчувствительности замедленного типа, в которых кроме Т-лимфоцитов участвуют макрофаги.
Гуморальный иммунный ответ подразумевает продукцию специфических антител в ответ на воздействие чужеродного антигена. Основную роль в реализации гуморального ответа играют В-лимфоциты, дифференцирующиеся под влиянием антигенного стимула в антителопродуценты. Как правило, В-лимфоциты нуждаются в помощи Т-хелперов и антиген-презентирующих клеток.
Особой формой специфического иммунного ответа на контакт иммунной системы с чужеродным антигеном является формирование иммунологической памяти, которая проявляется в способности организма отвечать на повторную встречу с тем же антигеном так называемым вторичным иммунным ответом – более быстрым и сильным. Эта форма иммунного ответа связана с накоплением клона долгоживущих клеток памяти, способных распознать антиген и ответить ускоренно и усиленно на повторный контакт с ним.
Альтернативной формой специфического иммунного ответа является формирование иммунологической толерантности – неотвечаемости на собственные антигены организма (аутоантигены). Она приобретается в период внутриутробного развития, когда функционально незрелые лимфоциты, потенциально способные разпознать собственные антигены, в тимусе вступают в контакт с этими антигенами, что приводит к их гибели или инактивации. Поэтому на более поздних стадиях развития иммунный ответ на антигены собственного организма отсутствует.
Взаимодействие нервной и иммунной систем.
Для двух основных регулирующих систем организма характерно наличие общих черт организации. Нервная система обеспечивает поступление и переработку сенсорных сигналов, иммунная - генетически чужеродной информации. В этой ситуации иммунный антигенный гомеостаз является компонентом в системе поддержания гомеостаза целостного организма. Поддержание гомеостаза нервной и иммунной системами осуществляется сопоставимым количеством клеточных элементов (1012 - 1013), а интеграция регулирующих систем в нервной системе осуществляется наличием отростков нейронов, развитого рецепторного аппарата, с помощью нейромедиаторов, в иммунной - наличием высокомобильных клеточных элементов и системы иммуноцитокинов. Подобная организация нервной и иммунной систем позволяет им получать, перерабатывать и сохранять полученную информацию (Петров Р.В., 1987; Адо А.Д. и др., 1993; Корнева Е.А. и др., 1993; Абрамов В.В., 1995). Поиск возможностей воздействия на течение иммунологических процессов через центральные регулирующие структуры нервной системы основывается на фундаментальных законах физиологии и достижениях иммунологии. Обе системы - нервная и иммунная - играют важную роль в поддержании гомеостаза. Последнее двадцатилетие отмечено обнаружением тонких молекулярных механизмов функционирования нервной и иммунной систем. Иерархическая организация регулирующих систем, наличие гуморальных механизмов взаимодействия клеточных популяций, точками приложения которых являются все ткани и органы, предполагают возможность обнаружения аналогий в функционировании нервной и иммунной систем (Ашмарин И.П., 1980; Лозовой В.П., Шергин С.М., 1981.; Абрамов В.В., 1995-1996; Jerne N.K., 1966; Cunningham A.J., 1981; Golub E.S., 1982; Aarli J.A., 1983; Jankovic B.D. et al., 1986, 1991; Fabry Z. et al., 1994).
В нервной системе полученная информация закодирована в последовательности электрических импульсов и архитектонике взаимодействия нейронов, в иммунной - в стереохимической конфигурации молекул и рецепторов, в сетевых динамических взаимодействиях лимфоцитов (Лозовой В.П., Шергин С.Н., 1981).
В последние годы получены данные о наличие общего рецепторного аппарата в иммунной системе к нейромедиаторам и в нервной системе к эндогенным иммуномодуляторам. Нейроны и иммуноциты снабжены одинаковыми рецепторными аппаратами, т.е. эти клетки реагируют на сходные лиганды.
Особое внимание исследователей привлекает участие медиаторов иммунитета в нейроиммунном взаимодействии. Считается, что помимо выполнения своих специфических функций внутри иммунной системы, медиаторы иммунитета могут осуществлять и межсистемные связи. Об этом говорит наличие рецепторов к иммуноцитокинам в нервной системе. Наибольшее количество исследований посвящено участию ИЛ-1, который не только является ключевым элементом иммунорегуляции на уровне иммунокомпетентных клеток, но и играет существенную роль в регуляции функции ЦНС.
Цитокин ИЛ-2 также оказывает множество различных эффектов на иммунную и нервную систему, опосредуемых путем аффинного связывания с соответствующими рецепторами клеточной поверхности. Тропность множества клеток к ИЛ-2 обеспечивают ему центральное место в формировании как клеточного, так и гуморального иммунного ответа. Активирующее влияние ИЛ-2 на лимфоциты и макрофаги проявляется в усилении антителозависимой цитотоксичности этих клеток с параллельной стимуляцией секреции ФНО-альфа. ИЛ-2 индуцирует пролиферацию и дифференцировку олигодендроцитов, влияет на реактивность нейронов гипоталамуса, повышает уровень АКТГ и кортизола в крови. Клетками-мишенями для действия ИЛ-2 служат Т-лимфоциты, В-лимфоциты, NК-клетки и макрофаги. Помимо стимуляции пролиферации, ИЛ-2 вызывает функциональную активацию этих клеточных типов и секрецию ими других цитокинов. Изучение влияния ИЛ-2 на NК-клетки показало, что он способен стимулировать их пролиферацию с сохранением функциональной активности, увеличивать продукцию NК-клетками ИНФ-гамма и дозозависимо усиливать NK-опосредованный цитолизис.
Существуют данные о продукции клетками центральной нервной системы (микроглией и астроцитами) таких цитокинов, как ИЛ-1, ИЛ-6 и ФНО-альфа. Продукция ФНО-альфа непосредственно в ткани мозга специфична для типичного нейроиммунологического заболевания - рассеянного склероза (РС). Повышение продукции ФНО-альфа в культуре изолированных ЛПС-стимулированных моноцитов/макрофагов наиболее отчетливо выявляется у больных с активным течением заболевания.
Установлена возможность участия в продукции интерферонов клеток мозга, в частности нейроглии или эпендимы, а также лимфоидных элементов сосудистых сплетений.
В процессе формирования иммунного ответа включаются нервные окончания в соответствующих лимфоидных органах. Инициирующие сигналы могут передаваться от иммунной системы в нервную гуморальным путем, в том числе, когда продуцируемые иммунокомпетентными клетками цитокины непосредственно проникают в нервную ткань и изменяют функциональное состояние определенных структур и описано проникновение через неповрежденный ГЭБ самих иммунокомпетентных клеток с последующей модуляцией функционального состояния нервных структур.
Иммунная система представляет собой совокупность всех лимфоидных органов и скоплений лимфоидных клеток тела, объединенных морфологически и функционально: лимфатические узлы, миндалины, селезенка, лимфоидные образования кожи и кишечника (аппендикс, пейеровы бляшки), лимфоциты костного мозга и крови. Все вместе они составляют единый «диффузный орган», объединенный общей функцией. Масса этого органа составляет 1% массы тела. Все клетки, осуществляющие иммунные реакции, называются имму- ноцитами. Они составляют 25-30% общего количества клеток крови у взрослых.
Различают центральные и периферические органы иммунной системы. Центральным органом иммунопоэза является костный мозг. Здесь на первоначальных стадиях дифференцировки из полипо- тентных стволовых клеток образуются лимфоидные стволовые клетки, из которых впоследствии возникают две клеточные популяции: Т-лимфоциты и В-лимфоциты. Тимус регулирует главным образом работу системы клеточного иммунитета (Т-системы). И в тимусе, и вне его Т-лимфоциты подвергаются регулирующему влиянию ви- лочковой железы.
Периферические органы иммунной системы представлены лимфоидными образованиями селезенки, лимфатических узлов кожи и другими образованиями (рис. 5.1).
Центральные органы иммунитета. Главным органом является костный мозг. Это поставщик самоподдерживающейся популяции поли- потентных стволовых клеток для всех ростков кроветворения, из которых развиваются лимфоциты, моноциты, гранулоциты, эритроциты, тромбоциты, макрофаги тканей. Подавляющее большинство костномозговых лимфоцитов - это В-лимфоциты, они могут выполнять функции предшественников плазматических клеток, т.е. антитело- продуцентов.
Рис. 5.1.
- 1 - кроветворный костный мозг; 2 - тимус; 3 - неинкапсулированная лимфоидная ткань слизистых оболочек; 4 - лимфатические узлы; 5 - сосуды лимфодренажа покровных тканей (афферентные лимфатические сосуды); 6 - грудной лимфатический проток (впадает в системную циркуляцию - кровь - через верхнюю полую вену);
- 7 - селезенка; 8 - печень; 9 - внутриэпителиальные лимфоциты
Лимфоидная стволовая клетка генерирует два типа клеток-пред- шественников Т- иВ-лимфоцитов, из которых и развиваются обе популяции лимфоцитов. Предшественники Т-лимфоцитов проходят через тимус, затем мигрируют в периферические лимфоидные органы, где под влиянием вилочковой железы достигают окончательной степени зрелости, превращаясь в сенсибилизированные лимфоциты.
Другая часть лимфоцитов созревает в аналоге фабрициевой сумки, превращаясь в В-лимфоциты, ответственные за синтез иммуноглобулинов.
Тимус (вилочковая железа) - центральный орган Т-системы иммунитета. Тимус отвечает за различные проявления клеточного иммунитета, осуществляемого не антителами, а лимфоцитами (противодействие патогенным грибам, вирусам, отторжение опухолей, чужеродных тканей, например, пересаженных органов). Предполагают, что часть тимопитов, находясь в вилочковой железе, взаимодействует с некоторыми тимусными эпителиальными клетками, избирательно экспрессирующими антигены II класса главного комплекса гистосовместимости, в результате чего «выживающие» Т-лимфоциты приобретают способность узнавать «свои» маркеры. Установлено, что в тимусе происходят элиминация клеток, способных реагировать против собственных антигенов (Т-клеточная толерантность), а также отбор Т-клеток, способных к одновременному распознаванию продуктов собственных МНС-генов вместе с чужеродными антигенами. Установлено, что сами тимоциты отличаются относительно низкой иммунологической активностью. Гормоны вилочковой железы индуцируют процессы созревания Т-лимфоцитов из Т-клеток-предшественников, способствуют превращению незрелых лимфоидных клеток и часто 0-лимфоцитов в Т-клетки; активируют или депрессируют клетки, генетически запрограммированные для дифференцировки в Т-лимфоциты.
Периферические органы иммунитета. Лимфатические узлы. Основная структурная единица лимфатического узла - лимфатический фолликул. Лимфатические узлы, как и тимус, содержат корковое и мозговое вещество. В корковом веществе находятся фолликулы, содержащие лимфоциты, макрофаги, плазмоциты, делящиеся клетки. В мозговом веществе фолликулов значительно меньше.
Лимфатические узлы выполняют целый ряд функций: это место образования лимфоцитов, здесь осуществляется синтез антител, происходит задержка различных чужеродных частиц и опухолевых клеток, а главное - здесь синтезируется значительное количество антител.
Селезенка. Построена аналогично тимусу и лимфатическим узлам. Основной структурный элемент - селезеночная долька. Лимфоидная ткань селезенки - белая пульпа, в ней есть тимуснезависимые и ти- мусзависимые зоны. В результате антигенной стимуляции в тимусза- висимых зонах образуются лимфобласты, а в тимуснезависимых происходит пролиферация лимфоцитов и образование плазматических клеток.
Лимфоидная ткань селезенки играет важную роль в резистентности организма к инфекциям и поддержании гомеостаза, так как в ней могут синтезироваться антитела.
Миндалины глоточного кольца. Находясь в начале дыхательного и пищеварительного трактов, они первыми соприкасаются со всевозможными антигенами, поступающими с пищей, водой и воздухом.
Ткань миндалин содержит Т- и В-лимфоциты. Благодаря значительной поверхности миндалин, макрофаги интенсивно взаимодействуют с антигенами, и через кровь и лимфу «информация» поступает в центральные органы иммунной системы. На поверхности миндалин кроме Т- и В-лимфопитов находятся иммуноглобулины различных классов, макрофаги, лизоцим, интерфероны, простагландины. Все это способствует осуществлению миндалинами местной защитной функции.
Лимфоидная ткань, ассоциированная со слизистыми оболочками. Данная лимфоидная ткань сокращенно обозначается как MALT (mucosal association lymphoid tissue). MALT является субэпителиальным скоплением лимфоидной ткани, не ограниченной соединительнотканной капсулой и расположенной в слизистой оболочке различных органов и систем (дыхательная, пищеварительная, мочевыделительная). В зависимости от этого выделяют BALT (bronchial associated lymphoid tissue), GALT(gastrointestinal associated lymphoid tissue) и другие подразделения системы MALT. Наиболее изучены ткани GALT-системы. Подавляющее большинство (95%) неагрегиро- ванных лимфоидных клеток диффузно расположены между эпителиальными клетками в слизистой оболочке пищеварительного тракта, причем в эпителиальном слое преобладают Т-цитотоксические лимфоциты, а в собственной пластинке - Т-хелперы. Плазматические клетки имеют тенденцию к скоплению в собственной пластинке слизистой оболочки. Примерно 85% их продуцирует иммуноглобулины А, 6-7% - иммуноглобулины М, 3-4% - иммуноглобулины G и менее 1 % - иммуноглобулины D и иммуноглобулины Е. В этом выражается основная роль лимфоидных образований слизистых оболочек - продукция димерного, секреторного иммуноглобулина A (SIgA).
Кровь относится также к периферическим органам иммунной системы. В ней циркулируют различные популяции лимфоцитов, моноциты, нейтрофилы.
Перечисленные органы, расположенные в различных частях тела, представляют собой единый диффузный орган и связаны между собой в цельную систему иммунитета сетью кровеносных и лимфатических сосудов с помощью медиаторов иммунитета, а также нервной и эндокринной систем.